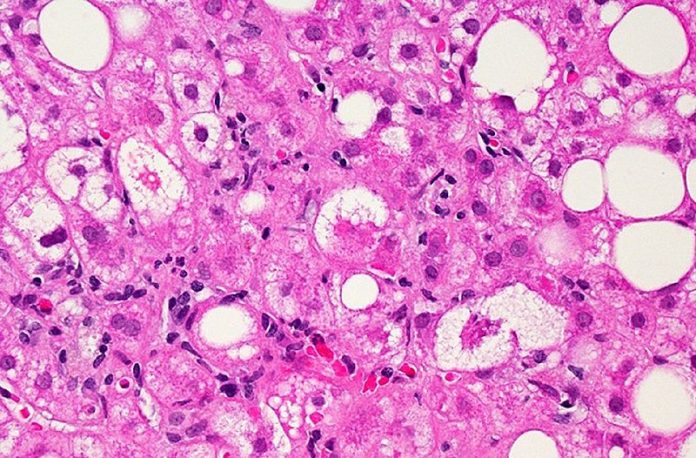
Rezdiffra (resmetirom) ला यूएसएच्या FDA द्वारे नॉन-अल्कोहोलिक नॉन-अल्कोहोलिक स्टीटोहेपेटायटिस (NASH) मध्यम ते प्रगत यकृताच्या जखमा (फायब्रोसिस) असलेल्या प्रौढांच्या उपचारांसाठी, आहार आणि व्यायामासह वापरण्यासाठी मान्यता दिली आहे.
आत्तापर्यंत, नॉन-सिरोटिक नॉन-अल्कोहोलिक स्टीटोहेपेटायटिस (NASH) असलेल्या रुग्णांना, ज्यांना यकृताचे लक्षणीय चट्टे आहेत, त्यांच्याकडे थेट उपचार करू शकणारे औषध नव्हते. यकृत नुकसान. एफडीएचा approval of Rezdiffra will, for the first time, provide a उपचार option for these patients, in addition to diet and exercise.
NASH नॉन-अल्कोहोलिक फॅटीच्या प्रगतीचा परिणाम आहे यकृत आजार जेथे यकृत जळजळ, कालांतराने, यकृताचे डाग आणि यकृत बिघडलेले कार्य होऊ शकते. NASH अनेकदा इतर आरोग्य समस्यांशी संबंधित आहे जसे की उच्च रक्तदाब आणि टाइप 2 मधुमेह. कमीतकमी एका अंदाजानुसार, यूएस मधील अंदाजे 6-8 दशलक्ष लोकांना मध्यम ते प्रगत यकृताच्या जखमांसह NASH आहे, ज्याची संख्या वाढण्याची अपेक्षा आहे.
रेझडिफ्रा हे थायरॉईड संप्रेरक रिसेप्टरचे आंशिक सक्रियक आहे; यकृतामध्ये रेझडिफ्राद्वारे या रिसेप्टरचे सक्रियकरण यकृतातील चरबीचे संचय कमी करते.
Rezdiffra ची सुरक्षा आणि परिणामकारकता
12 महिन्यांच्या यादृच्छिक, डबल-ब्लाइंड प्लेसबो-नियंत्रित चाचणीमध्ये 54 महिन्याच्या सरोगेट एंडपॉईंटच्या विश्लेषणाच्या आधारे रेझडिफ्राची सुरक्षितता आणि परिणामकारकतेचे मूल्यांकन केले गेले. सरोगेट एंडपॉइंटने ची व्याप्ती मोजली यकृत जळजळ आणि डाग. प्रायोजकाने Rezdiffra च्या क्लिनिकल फायद्याची पडताळणी आणि वर्णन करण्यासाठी अनुमोदनानंतरचा अभ्यास करणे आवश्यक आहे, जो समान 54-महिन्यांचा अभ्यास पूर्ण करून केला जाईल, जो अजूनही चालू आहे. चाचणीमध्ये नावनोंदणी करण्यासाठी, रुग्णांना ए यकृत मध्यम किंवा प्रगत सह NASH मुळे जळजळ दर्शवणारी बायोप्सी यकृत डाग चाचणीमध्ये, 888 विषयांना यादृच्छिकपणे खालीलपैकी एक प्राप्त करण्यासाठी नियुक्त केले गेले: प्लेसबो (294 विषय); 80 मिलीग्राम रेझडिफ्रा (298 विषय); किंवा 100 मिलीग्राम रेझडिफ्रा (296 विषय); दररोज एकदा, NASH साठी मानक काळजी व्यतिरिक्त, ज्यामध्ये निरोगी आहार आणि व्यायामासाठी समुपदेशन समाविष्ट आहे.
12 महिन्यांत, यकृताच्या बायोप्सीने असे दिसून आले की ज्यांना प्लॅसिबो मिळालेल्या लोकांच्या तुलनेत रेझडिफ्राने उपचार घेतलेल्या लोकांच्या मोठ्या प्रमाणात NASH रिझोल्यूशन किंवा यकृताच्या डागांमध्ये सुधारणा झाली. एकूण 26% ते 27% रुग्ण ज्यांना 80 मिलीग्राम रेझडिफ्रा आणि 24 मिलीग्राम रेझडिफ्रा मिळालेल्या 36% ते 100% रुग्णांना NASH रिझोल्यूशनचा अनुभव आला आणि यकृताच्या जखमा बिघडल्या नाहीत, 9% ते 13% लोकांच्या तुलनेत प्लॅसिबो आणि आहार आणि व्यायामाबद्दल समुपदेशन प्राप्त केले. प्रतिसादांची श्रेणी वेगवेगळ्या पॅथॉलॉजिस्टचे वाचन प्रतिबिंबित करते. याव्यतिरिक्त, एकूण 23% ज्यांना 80 मिलीग्राम रेझडिफ्रा आणि 24% ते 28% ज्यांना 100 मिलीग्राम रेझडिफ्रा प्राप्त झाले त्यांच्यामध्ये सुधारणा दिसून आली. यकृत प्रत्येक पॅथॉलॉजिस्टच्या रीडिंगनुसार प्लेसबो मिळालेल्या 13% ते 15% लोकांच्या तुलनेत NASH चे डाग पडणे आणि खराब होत नाही. केवळ एक वर्षाच्या उपचारानंतर रुग्णांच्या प्रमाणात या बदलांचे प्रात्यक्षिक लक्षणीय आहे, जसे की आजार सामान्यत: हळूहळू प्रगती होते, बहुतेक रुग्णांना प्रगती दाखवण्यासाठी वर्षे किंवा अगदी दशके लागतात.
Rezdiffra चे दुष्परिणाम
Rezdiffra च्या सर्वात सामान्य दुष्परिणामांमध्ये अतिसार आणि मळमळ यांचा समावेश होतो. रेझडिफ्रा काही इशारे आणि खबरदारी घेऊन येते, जसे की औषध-प्रेरित यकृत विषारीपणा आणि पित्ताशय-संबंधित दुष्परिणाम.
विघटित सिरोसिस असलेल्या रुग्णांमध्ये रेझडिफ्रा चा वापर टाळावा. रुग्णांना बिघडण्याची चिन्हे किंवा लक्षणे आढळल्यास रेझडिफ्रा वापरणे थांबवावे यकृत रेझडिफ्रा उपचार चालू असताना कार्य.
रेझडिफ्रा च्या औषध संवाद
कोलेस्टेरॉल कमी करण्यासाठी काही इतर औषधांप्रमाणेच रेझडिफ्रा वापरणे, विशेषत: स्टॅटिन्स, संभाव्यत: महत्त्वपूर्ण औषध परस्परसंवाद होऊ शकतात. आरोग्य सेवा प्रदात्यांनी रेझडिफ्रा, शिफारस केलेले डोस आणि प्रशासनातील बदलांवरील संभाव्य महत्त्वपूर्ण औषधांच्या परस्परसंवादावरील अतिरिक्त माहितीसाठी संपूर्ण विहित माहितीचा संदर्भ घ्यावा.
अगोदर निर्देश केलेल्या बाबीसंबंधी बोलताना अन्न व औषध प्रशासनाचे रेझडिफ्राला प्रवेगक मंजूरी मार्ग अंतर्गत मंजूरी दिली आहे, जी गंभीर परिस्थितींवर उपचार करणाऱ्या आणि वैद्यकीय फायद्याचा अंदाज लावण्याची वाजवी शक्यता असलेल्या सरोगेट किंवा इंटरमीडिएट क्लिनिकल एंडपॉईंटवर आधारित, अपुऱ्या वैद्यकीय गरजा पूर्ण करणाऱ्या औषधांना पूर्वीच्या मंजुरीसाठी परवानगी देते. आवश्यक उपरोक्त 54-महिन्यांचा अभ्यास, जो चालू आहे, 54 महिन्यांच्या रेझडिफ्रा उपचारानंतर क्लिनिकल फायद्याचे मूल्यांकन करेल.
रेझडिफ्राला या संकेतासाठी ब्रेकथ्रू थेरपी, फास्ट ट्रॅक आणि प्राधान्य पुनरावलोकन पदनाम मिळाले आहेत.
अगोदर निर्देश केलेल्या बाबीसंबंधी बोलताना अन्न व औषध प्रशासनाचे माद्रिगल फार्मास्युटिकल्सला रेझडिफ्रा ची मान्यता दिली.
***
स्त्रोत:
FDA 2024. बातमी प्रकाशन - FDA ने फॅटी लिव्हर डिसीजमुळे लिव्हर स्कारिंग असलेल्या रूग्णांसाठी पहिल्या उपचारांना मान्यता दिली. 14 मार्च 2024 रोजी पोस्ट केले. येथे उपलब्ध https://www.fda.gov/news-events/press-announcements/fda-approves-first-treatment-patients-liver-scarring-due-fatty-liver-disease
***